欧盟授权代表EAR(European Authorised Representative) 是指由位于欧洲经济区EEA(包括EU与EFTA)境外的制造商明确指定的一个自然人或法人,该自然人或法人可代表EEA境外的制造商履行欧盟相关法律对该制造商所要求的特定职责,并全权承担法律所要求的在EEA区域或欧共体内部关于产品安全性和一致性的责任。

自2021年7月起,位于欧盟以外但在欧盟境内进行企业对个人销售的公司必须具有授权的代表。授权代表的职责可概括如下:
授权代表授权非欧盟公司在产品包装上使用授权代表的欧洲地址(此为强制规定)
授权代表持有技术文件、测试报告及其他相关的合规性文件
授权代表以非欧盟公司的名义与国家主管部门(例如市场监督部门)进行沟通
受制造商的委托,在欧盟进行产品注册,申请欧盟颁发的自由销售证书(CFS/FSC)
非欧盟企业在没有授权代表地址的情况下在欧盟境内进行销售活动,海关当局有权没收和销毁入境货物。
我们AAMedTech GmbH作为欧盟授权代表能够代为非EEA制造商履行欧盟相关法律对该制造商所要求的特定职责并提供产品的CE认证。
CE认证是欧盟的产品安全认证,所有进入欧盟市场的医疗器械都必须进行医疗器械CE认证。医疗器械需要满足的CE指令现已全部升级为法规,分别是:
Medical Device Regulation
根据欧盟对医疗器械产品的分类标准,I类(灭菌/测量/可重复使用)、IIa类、IIb类和III类医疗器械制造商在使用CE标志并在市场上投放产品之前,必须从公告机构获得符合MDR (EU) 2017/745的CE标志认证;I类中,除灭菌/测量/可重复使用之外的产品,可以自我声明方式获得CE标志认证。
In Vitro Diagnostic Regulation
根据欧盟对体外诊断医疗器械产品的分类标准,A类(需要灭菌的)、B类、C类和D类IVD医疗器械制造商在使用CE标志并在市场上投放产品之前,必须从公告机构获得符合IVDR (EU) 2017/746的CE标志认证;A类非灭菌IVD产品,可以自我声明方式获得CE标志认证。
体系认证是ISO国际标准化组织制订的相关管理的体系认证,通过体系认证可直观反映企业的质量、生产环境控制、从业人员职业健康等管理水平等,从而达到对现代企业管理要求的及格标准。应该说,管理体系良好运转,是企业提供良好产品和服务的必然保证。
我们可以承接下列体系的辅导与认证:





以下列出了我们在欧代服务领域的部分具有代表性的案例

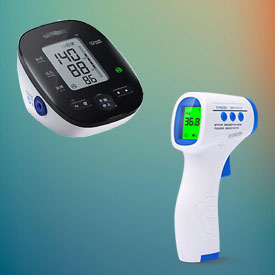

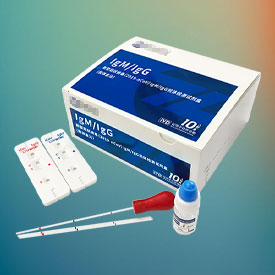
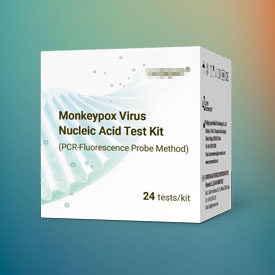








请把您的 Email 发给我们,我们会安排专人反馈您。
一般情况下,一周内即可办理完手续。
同一个产品只能有一个欧盟授权代表。如果您销售多种类别的产品,则可能需要指定多个授权代表。例如,如果您销售的产品分为“玩具”类别和“电子产品”类别,则可能需要为每个类别分别指定一个授权代表。
“授权代表”是代表厂商履行与CE条例规定的义务相关的特定职责的。“进口商”是将来自第三国的器械设备投放欧盟市场的。“分销商”是指供应链中除厂商和进口商以外的将器械设备在市场上供货至投入使用一刻的任何自然人或法人。三者的职责范围是明显不同的,其次每个厂商同一个产品只允许有一个授权代表,但是进口商和销售商(分销商)可以有多个。
CE认证即欧洲合格认定。欧洲合格认证规定大部分在欧洲经济区(EEA)销售的产品,都需要印上“CE”标志。该标志代表产品制造商或服务提供者确保产品符合相应的欧洲联盟指令、且已完成相应的评估程序。相关欧盟指令包括医疗器械、玩具安全、机械工具等指令。现时约有25条指令要求产品印上“CE”标志。
不能。自英国脱欧以后,产品销往英国需要有英国负责人(职责类似于欧盟授权代表)并通过英国UKCA认证(医疗器械还需完成MHRA注册)。如您有相关需求,也可以联系我们获取相关服务。
欢迎您在下方表单留言以跟我们取得联系,我们将会尽快回复您。